أعلنت شركة Suzhou CH Biomedical عن موافقة إدارة الغذاء والدواء الأمريكية (FDA) لبدء التجارب السريرية لنظام المساعدة البطينية اليسرى BrioVAD™، والذي يعد بحلول مبتكرة لفشل القلب.


مؤخراً، أعلنت شركة Suzhou CH Biomedical، Inc. أن نظام المساعدة البطينية اليسرى التالي من الجيل الجديد، BrioVAD™، الذي يعمل بشكل كامل على الرفع المغناطيسي، قد حصل على موافقة إدارة الغذاء والدواء الأمريكية لإجراء التجارب السريرية. وقد حصلت التجربة السريرية المبتكرة، التي تحمل اسم INNOVATE، على إعفاء الجهاز التجريبي (IDE) من FDA، مما يسمح ببدء تجنيد المرضى بشكل مشروط.
ستقوم هذه الدراسة بتقييم فعالية وأمان BrioVAD™، وهو نظام المساعدة البطينية اليسرى الذي يعمل بالكامل على الرفع المغناطيسي، في معالجة فشل القلب المقاوم. في الوقت نفسه، عقدت شركة CH Biomedical أول اجتماع للباحثين للدراسة وبدأت الأعمال الأولية المتعلقة بمراكز التجارب السريرية في الولايات المتحدة.

▲ شركة CH Biomedical تعقد أول اجتماع للباحثين لتجربة INNOVATE السريرية
نظام المساعدة البطينية اليسرى BrioVAD™، الذي حصل على موافقة FDA في الولايات المتحدة، يبني على التوافق الممتاز للدم للمنتج الحالي، CH-VAD. من خلال عدة ابتكارات تكنولوجية، يحقق قابلية حمل المكونات الخارجية بينما يعزز أداء النظام بشكل عام. بالإضافة إلى ذلك، ستستخدم دراسة INNOVATE تصميمًا عشوائيًا محكومًا لمقارنة وتقييم BrioVAD™ مع المنتجات التي تمت الموافقة عليها مسبقًا من قبل FDA.
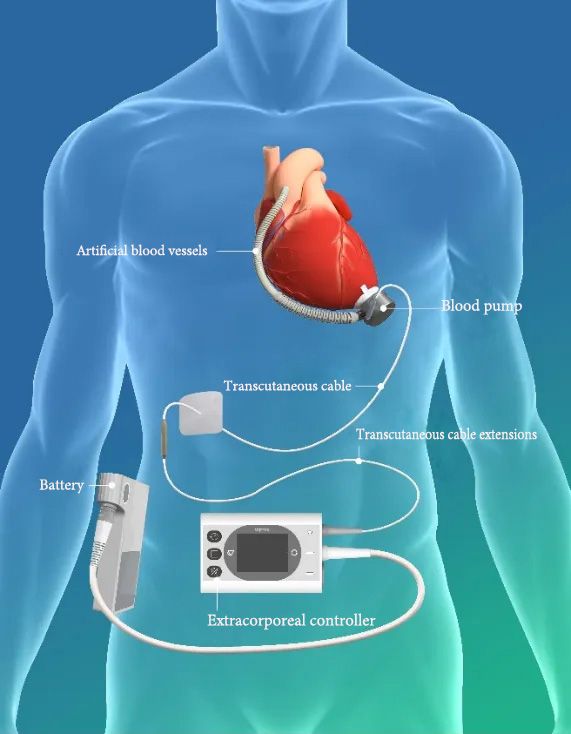
▲ الرسم البياني لمنتج نظام المساعدة البطينية اليسرى BrioVAD™
CH-VAD هو أول جهاز مساعد بطيني يساري مغناطيسي كامل الرفع تم تطويره محليًا في الصين. تم تطويره بشكل مشترك بواسطة فريق مستشفى فوى ومؤسسة CH Biomedical، ويزن 186 جرامًا، بقطر مضخة الدم 50 ملم، وسمك 26 ملم، وأقصى معدل تدفق 10 لتر/دقيقة. التقنية الأساسية لهذا المنتج تتضمن بشكل رئيسي تكنولوجيا مضخة الدم المغناطيسية الكاملة، والتي حصلت على براءات اختراع متعددة في الصين والولايات المتحدة، مما يجعلها جهازًا طبيًا مبتكرًا محليًا. مقارنةً بالمنتجات الدولية المماثلة، فإن مؤشرات الأداء الرئيسية لها وصلت إلى نفس المستوى، مع حجم مضخة أصغر وتأثير أفضل على الغزو.
تتوفر CH-VAD سريريًا منذ عام 2018 وتلقت موافقة NMPA لاستخدامها مع الأوعية الدموية الاصطناعية المحددة في عام 2021، مما يوفر دعمًا ميكانيكيًا للدورة الدموية للمرضى في مرحلة النهاية من فشل القلب المقاوم، وتستخدم كعلاج انتقالي قبل زراعة القلب أو لاستعادة وظيفة القلب.

▲ نظام المساعدة البطينية اليسرى القابل للزراعة (CH-VAD)
يتكون CH-VAD من مكونات زرع داخلية، ومكونات حمل خارجية، ومكونات محيطية، وأدوات جراحية متخصصة. إنه جهاز كهربائي ميكانيكي متكامل يُستخدم لتعويض وظيفة ضخ القلب جزئيًا والحفاظ على الدورة الدموية البشرية. المكون الأساسي له هو مضخة الدم التي تسحب الدم من القلب، وتزيد من ضغطه، وتوصله إلى الشريان الأورطي، مما يقلل من عبء العمل الطبيعي للقلب، مما يسمح له بالراحة، بينما يعزز القدرة الطبيعية للقلب على الضخ.
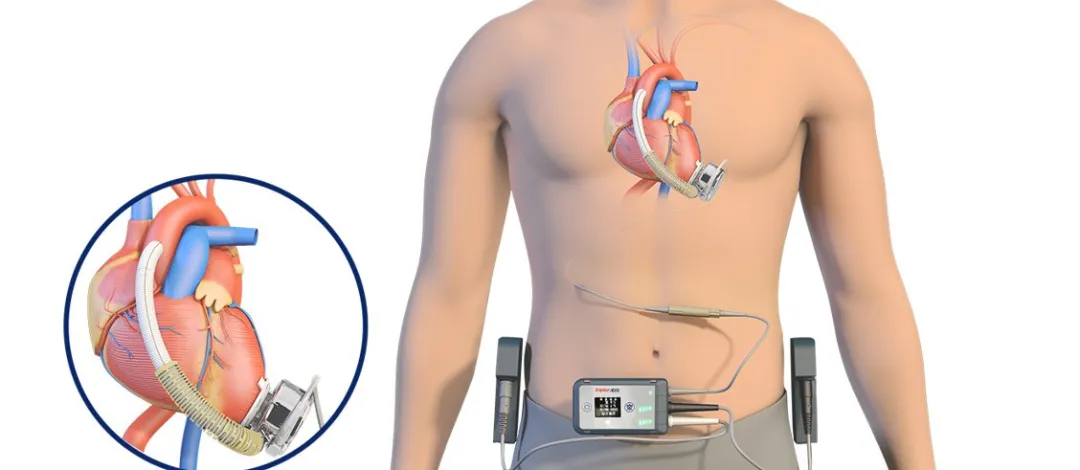
▲ نظام المساعدة البطينية اليسرى القابل للزراعة (CH-VAD)
منذ إطلاقه، تم استخدام CH-VAD في أكثر من 180 مريضًا في أكثر من 40 مستشفى للقلب الرائدة في البلاد. نجى المريض الأول لأكثر من 6 سنوات واستمر في قيادة حياة عالية الجودة. يمتلك CH-VAD نظام حقوق ملكية فكرية مستقلة كاملة مبنية من الصفر وقد حصل على حماية براءات الاختراع في الصين، والولايات المتحدة، وأوروبا، واليابان، ودول ومناطق أخرى.
في أبريل 2024، في ندوة ISHLT بعنوان "Spin Doctors and Heart Hotties: Unleashing the Future of MCS Devices"، قدم الأستاذ شيانكيانغ وانغ من مستشفى فوى، الأكاديمية الصينية للعلوم الطبية، نتائج المتابعة طويلة الأجل لـ CH-VAD على المستوى الدولي. في هذه الدراسة المراجعية القائمة على مركز واحد، أظهرت نتائج فشل القلب في مرحلة النهاية التي عولجت بـ CH-VAD معدلات بقاء عالية ومعدلات مضاعفات منخفضة، دون حدوث حالات من تخثر المضخة، السكتات الدماغية المعوقة، أو الفشل الكبير للجهاز.
أهداف البحث
لتقييم فعالية وأمان CH-VAD على المدى الطويل، أجرت مستشفى فوى هذه الدراسة المراجعية القائمة على مركز واحد، بما في ذلك المرضى المصابين بفشل القلب الذين عولجوا بـ CH-VAD من يونيو 2017 إلى أغسطس 2023، لتحليل بياناتهم السريرية وتوقعاتهم طويلة الأجل إحصائيًا.
طرق البحث
شملت هذه الدراسة 50 مريضًا مع مدد متابعة تتراوح من 3 أشهر إلى 6.7 سنوات. كان متوسط مدة دعم المضخة للمرضى 2.4 سنوات، وقد خضع جميع المرضى بنجاح لزراعة LVAD. كانت عملية تشغيل مضخة الدم للمرضى مستقرة سواء أثناء العملية أو بعدها، وعادت الديناميكا الدموية إلى طبيعتها.
نتائج البحث
باستخدام تحليل بقاء Kaplan-Meier، كانت معدلات البقاء عند 1 سنة، و2 سنة، و3 سنوات للمرضى 93%، و93%، و89% على التوالي، جميعها أعلى من تلك الموجودة في الدراسات السريرية الدولية والإعدادات الواقعية. من بين الـ 50 مريضًا، خضع اثنان فقط لزراعة القلب كحل وسيط. استعادة وظيفة القلب بالكامل وتم إزالة LVAD في ثلاث حالات.
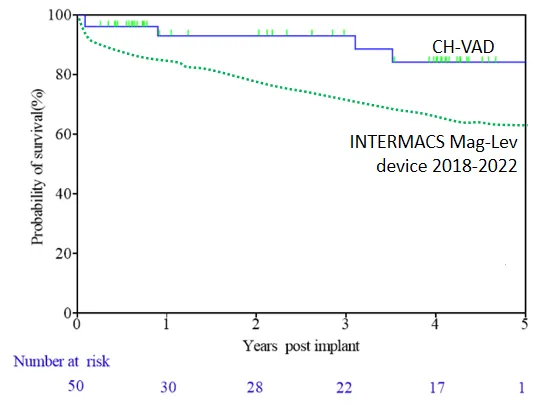
▲ بقاء المرضى خلال المتابعة
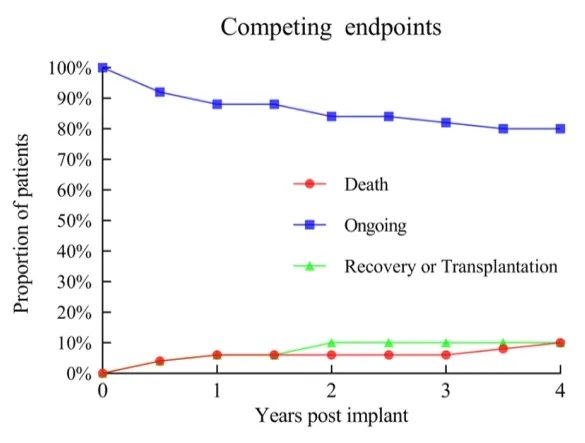
▲ حدوث الأحداث لنقاط النهاية المختلفة
في هذه الدراسة، كانت نسبة حدوث الأحداث السلبية الإجمالية منخفضة. تجلى التوافق الممتاز للدم لـ CH-VAD، حيث لم تُلاحظ حالات تخثر المضخة، أو انحلال الدم، أو أحداث السكتة الدماغية المعوقة.
من بين جميع المرضى، عانى اثنان فقط من السكتات الدماغية الإقفارية (0.02 لكل شخص في السنة)، وعانى واحد من سكتة دماغية نزفية (0.01 لكل شخص في السنة)، واستعادت جميع وظائف المرضى العصبية خلال المتابعة. كانت أكثر الأحداث السلبية شيوعًا هي العدوى بعد العملية، والتي تم منعها والتحكم فيها بشكل فعال من خلال تراكم خبرة الإدارة بين التخصصات، مما أدى إلى توقعات جيدة لأغلب المرضى. لم تكن هناك حالات فشل كبير للجهاز أو جراحة استبدال المضخة خلال فترة المتابعة، مما يشير إلى موثوقية طويلة الأجل عالية للجهاز.
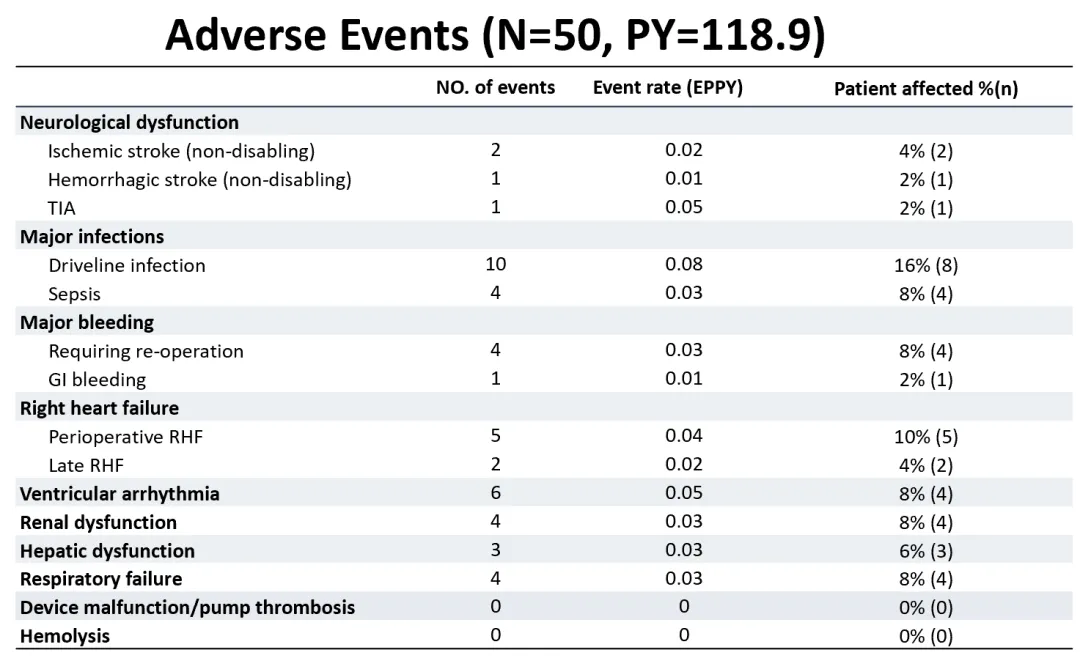
▲ حدوث أنواع مختلفة من الأحداث السلبية
في 15 أبريل 2024، أعلنت إدارة الغذاء والدواء الأمريكية (FDA) عن استدعاء نظم المساعدة البطينية اليسرى HeartMate II وHeartMate 3 التي تصنعها Abbott/Thoratec بسبب حدوث انسداد في المخرج الناتج عن قوى خارجية. أثر هذا الاستدعاء على 13,883 جهازًا، مما يمثل 56% من إجمالي المنتجات في السوق، مع معدل حدوث تقديري بناءً على Kaplan-Meier بنسبة 0.24% عند سنتين و2.06% عند خمس سنوات لـ HeartMate 3 EOGO.
تعد حوادث EOGO المرتبطة بـ HeartMate II وHeartMate 3 في هذا الاستدعاء ليست جديدة على الصناعة. حتى الآن، تلقت FDA العديد من تقارير الأحداث السلبية المتعلقة بـ EOGO مع HeartMate، بلغ إجماليها 273 حالة إصابة و14 حالة وفاة.
من الجدير بالذكر: أولاً، لا يعني استدعاء من الفئة الأولى من قبل FDA للأجهزة الطبية توقف الإنتاج أو استخدام المنتج، بل يتعين اتخاذ إجراءات تصحيحية للمشاكل المحددة، وستستمر الأجهزة في الاستخدام في الأوساط السريرية. ثانيًا، سبب الاستدعاء من الفئة الأولى لـ HeartMate II وHeartMate 3 من قبل FDA هو EOGO، الناتج عن غلاف تدعيم مادة PTFE الكثيف لـ HeartMate II وHeartMate 3، مما يتسبب في تراكم المواد البيولوجية غير الخلوية، مما يجبر الوعاء الدموي الاصطناعي على الضغط نحو الداخل. ومع ذلك، فقد حلت الأجهزة المحلية LVAD التي يمثلها CH-VAD العيوب التصميمية المذكورة أعلاه لـ HeartMate من خلال التصميم المجوف للغلاف التدريجي.
تتيح تقنية الرفع المغناطيسي دورانًا مستقرًا بدون الحاجة إلى ظروف سائلة، مما يقلل بشكل كبير من تلف الدم، وبالتالي تقليل حدوث المضاعفات ذات الصلة مثل التخثر والسكتة الدماغية. يحقق CH-VAD تعليقًا مستقرًا في خمسة درجات من الحرية على المحاور X وY وZ عن طريق ترتيب المولد الثابت والمولد المغناطيسي الثابت على جانبي الدوار، مما يضمن مقاومة جيدة للصدمات وتشغيلًا مستقرًا على المدى الطويل، مما يقلل من تلف الدم. في الوقت نفسه، يضمن تصميم قناة التدفق المحسن تدفق الدم السلس من الأنبوب المدخل إلى موضع الدافع عبر مخروط أنفي، مع قناة تدفق ثانوية على شكل U بفجوة 250 ميكرون، مما يضمن كل من تدفق الدم السلس وتأثيرات غسل جيدة.
أشار الأستاذ زينغشينغ تشين من جامعة بيهانغ إلى أن "السبب" وراء هذا الاستدعاء يكمن في غلاف تدعيم مادة PTFE الكثيف لـ HeartMate II وHeartMate 3، بينما حلت الأجهزة المحلية LVAD التي يمثلها CH-VAD مشكلة الضغط على الأوعية الاصطناعية من خلال التصميم المجوف للغلاف التدريجي.
تُعتبر مضخات VAD اليوم من أحدث التقنيات القابلة للزرع. خذ على سبيل المثال CH-VAD. إنها مزودة بمروحة رائعة، وهي جزء متحرك واحد يدفع الدم بكفاءة في اتجاه واحد. معلقة بالمغناطيسات، تعمل هذه المروحة بدون احتكاك ولا تحتوي على مكونات عرضة للتآكل.
تلعب المراوح دورًا حاسمًا في VADs. عندما يمر التيار عبر المغناطيسات، تبدأ المروحة في الدوران. يتم جذب الدم إلى مركز المروحة تحت ضغط سلبي، وتسرع شفراتها الدوارة الدم بسرعة من المركز إلى الأطراف. يتدفق الدم المحول، الآن تحت ضغط إيجابي، من المضخة عبر فوهة التفريغ إلى الأنبوب الخارج.
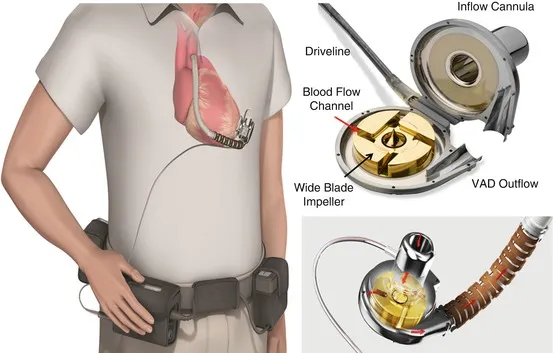
▲ مروحة مضخة الدم في VAD
تصميم المروحة أمر بالغ الأهمية. تمسكها المغناطيسات والمحامل المتخصصة، وتدور بسلاسة دون لمس الجوانب. يضمن هذا التصميم ليس فقط تقليل التلف ولكن أيضًا طول عمر الجهاز.
في Manners Technology، نتخصص في صناعة أجزاء للأجهزة الطبية، بما في ذلك المراوح لمضخات VAD. يتميز التزامنا بالجودة بشهاداتنا، بما في ذلك ISO 9001:2015 وISO 13485.
نتعاون أيضًا مع شركة ألمانية رائدة لتطوير مراوح أكثر كفاءة وموثوقية لمضخات VAD. معًا، نسعى لإنتاج أجزاء تتجاوز التوقعات. سواء كنت بحاجة إلى أجزاء متخصصة أو مساعدة في التصميمات، فإن خدماتنا المخصصة مصممة لتلبية احتياجاتك.